目次
20世紀に誕生した量子力学
20世紀に誕生した量子力学。量子とは物質の小さな単位で、ここには原子、分子、そして電子や光子も含まれる。つまり量子力学とは、これらの本質を理解しようとするため20世紀初頭の天才物理学者たちが考え抜いた、理論と実験の積み重ねの成果である。量子の世界では、これまで(19世紀)の物理学ではまったく説明できない部分があった。そこを解明しつつあるのが、量子の特性を解明する量子力学だ。これが一応の完成を見たのが、1926年のシュレーディンガーの波動方程式の発見によってだった。この間に原子と分子の中身、それと電波や光、X線のような電磁波との関係について多くのことが分かってきた。
量子力学では原子の構造はどんなものかについて多くの研究がなされ、いくつかの提案が生まれた。
今、原子構造というと、中心に核があり、そのまわりを電子が回っているという絵を思い出す。中心に丸が描かれていて、その他にもう1つの丸があり、楕円が4つその周りを囲んでいるものだ。
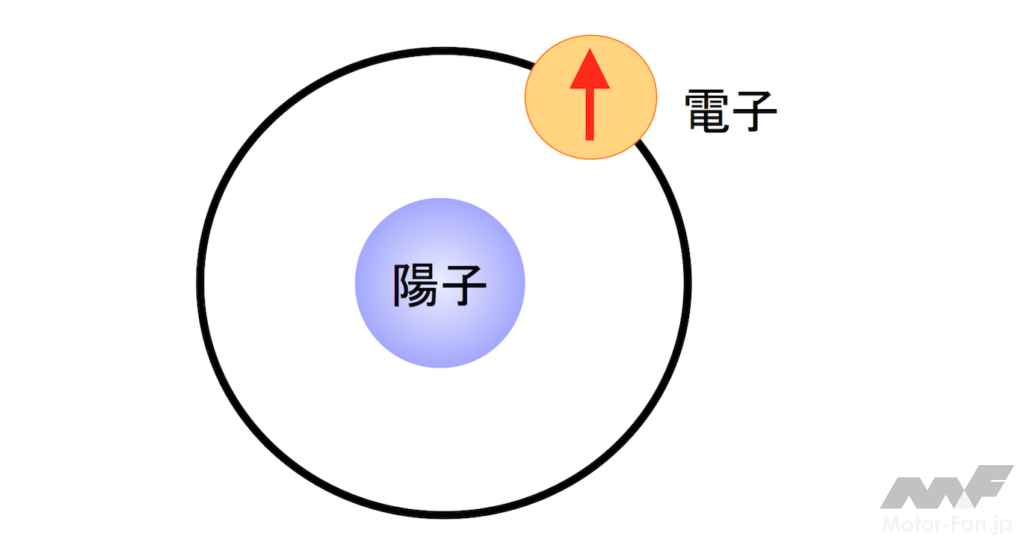
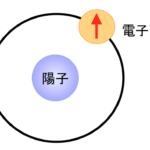
この構造で核はプラスの電気を持ち、これが陽子である。水素以外の原子では陽子と同じ重さの中性子がある。回っている電子は原子からの距離が一定のところに存在し、そこが電子軌道である。電子はマイナスの電気を持っている。原子で最も単純な構造をしているのは水素であるが、陽子が1個と原子が1個である。水素は核の最も近い円形の軌道を回っている。
次に単純なのがヘリウムで、陽子が2個に電気的には中性の中性子が2個、それに電子が同じ円形の軌道を2個回っている。3個目のリチウムでは電子は3個で、3個目の電子は円形の軌道の外側にある楕円の軌道を回る。こうして原子番号10のネオンまでは楕円形の軌道を回る。
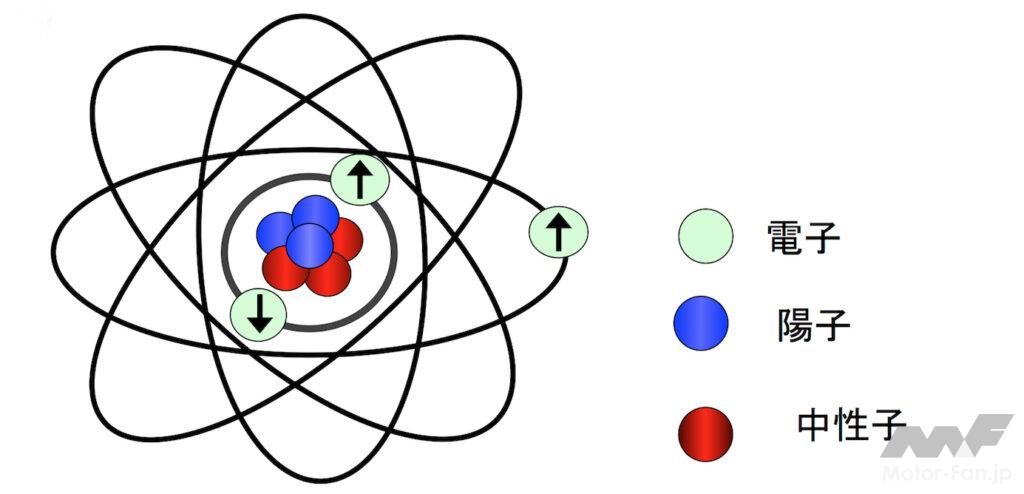
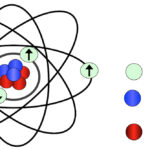
次はナトリウムになるが、これは11番目の電子が3つ目の軌道を回る。この軌道はリボンで輪を描いてその中心をピンで止めたような形になり、ピンに相当する位置が核となる。この軌道を使って電子が回るのは18番目のアルゴンまでである。
量子の性質は波のようでもあり粒のようでもある
量子力学では、あらゆる物質は「波のような性質」と「粒のような性質」もあると解釈すると実際の現象が説明できることが分かった。このため原子の正確な形も軌道上を粒状の電子が回っているのではなく、薄い雲のように波の形をしたものが覆っていると考えるのがより正確である。しかし人の頭では粒状の電子が回っていると解釈する方が分りやすいため、このような表現がなされている。
分子は原子の集合体であることも明らかになり、分子が出来るためには軌道を回る電子の数が軌道に入ることができる電子の数を満たした時であることも分かった。これで化学変化が起こる理由も理解できた。
また物質に光を含む電磁波が当たると、これが吸収されたり、反射されたり、そのまま透過するのはなぜかも理解できてきた。そして光も波のような性質と粒のような性質も持つと捉えると、現象が説明できることが分かったことも量子力学の重要な成果である。
また物質はその存在する場所を正確に捉えようとすると、そこに居る時間がいつかがあいまいになったり、居る時間を捉えようとすると、その場所があいまいになるという不確定性原理も生まれた。
こうして原子と分子及び電磁波の関係が人間の頭の中ですっきり分かるようになった。そして、これらの現象を統一的に表現したのがシュレーディンガーの波動方程式である。さらに、量子力学の発展が20世紀の新たな発明とそれに基づく技術を生み出す原動力になった。脱・温暖化の鍵として、ここに注目するべきなのではないか、と考えている。